En 1825, un composé chimique assez singulier est isolé par le célèbre physicien Michael Faraday. Il s’agit du benzène alors utilisé dans les bouteilles d’éclairage et dont la structure correcte n’a été définie précisément qu’en 1933 par le chimiste Linus Pauling.
Ceci dit, depuis que la molécule a été découverte, les scientifiques ne sont jusque là pas parvenus à trouver sa structure électronique connue pour être particulièrement complexe.
Ce débat qui fait rage depuis près de 200 ans vient toutefois d’être résolu pour donner lieu à des avancées importantes en matière de développement de matériaux optoélectroniques.
L’étude publiée dans la revue Nature Communications indique que le benzène possède une structure atomique simple et bien assimilée par les experts avec un cycle qui se compose de six atomes d’hydrogène et six atomes de carbone.
La difficulté réside dans le nombre d’électrons contenus dans la molécule qui s’élève à 42 et qu’il faut considérer. Timothy Schmidt, Professeur de l’Université de Sydney, déclare que ceux renfermés dans le benzène sont décrits par une fonction mathématique de 126 dimensions différentes, soit 3 pour chaque électron.
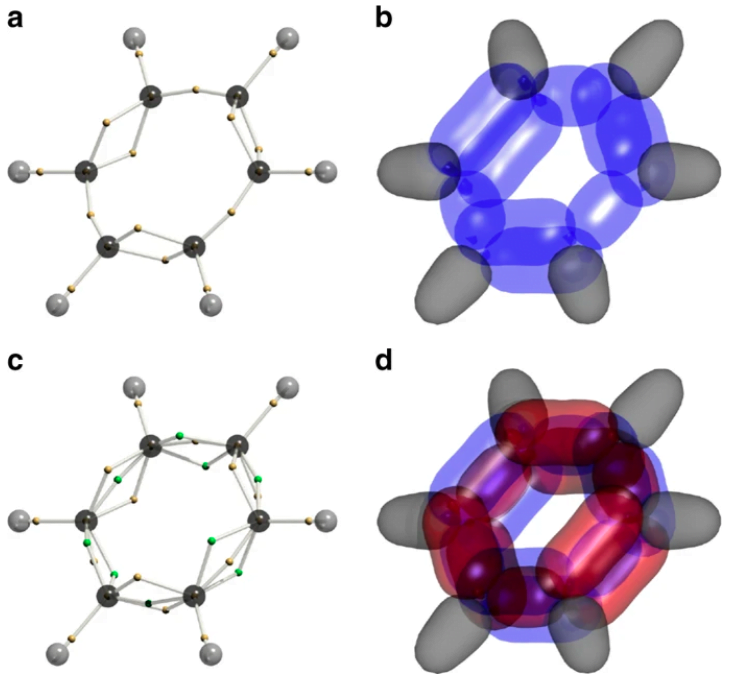
Nature Communications
C’est cette complexité qui a rendu impossible la révélation de la structure électronique du benzène durant toutes ces années. Toutes les théories mises en place dans le but de percer ce mystère ont fini par échouer.
L’équipe derrière cette trouvaille s’est basée sur une nouvelle technique récemment élaborée. Appelée échantillonnage dynamique de Voronoi Metropolis, cette approche algorithmique sert à afficher les fonctions d’onde d’un système à électrons multiples et de séparer les 126 dimensions dans un diagramme pour être cartographiées.
« La fonction mathématique qui décrit les électrons du benzène est de 126 dimensions. Cela signifie que c’est une fonction de 126 coordonnées, trois pour chacun des 42 électrons. Les électrons ne sont pas indépendants, nous ne pouvons donc pas le décomposer en 42 fonctions tridimensionnelles » déclare M. Schmidt.
Il explique également que les électrons avec un spin haut à double liaison étaient identiques à ceux avec un spin bas à simple liaison, et inversement. Lorsque la situation le nécessite, cela les incitera à s’éloigner les uns des autres, ce qui aura pour effet de réduire l’énergie du benzène et de le rendre plus stable.
Les résultats de cette étude ont ainsi offert la possibilité de comprendre la corrélation électronique du benzène. Il est à présent clair que les électrons ne sont pas assemblés dès que la condition énergétique devient avantageuse.